Sn
Stannum
ESTAÑO
GRUPO DEL CARBONO
| Número atómico: | 50 |
| Grupo: | 14 |
| Periodo: | 5 |
| Configuración electrónica: | [Kr] 4d10 5s2 5p2 |
| Estados de oxidación: | +2 +4 |
| Electronegatividad: | 1.96 |
| Radio atómico / pm: | 140.5 |
| Masa atómica relativa: | 118.710(7) |
Las aleaciones de cobre y estaño dan nombre a una época prehistórica (la Edad del Bronce). El símbolo Sn viene del latín 'stannum'. Es un metal color blanco plateado, suave, dúctil y maleable. Se utiliza para recubrir las latas de acero ya que no es tóxico ni corrosivo. Los compuestos de estaño se usan para fungicidas, tintes, dentífricos (SnF2) y pigmentos.
| Densidad / g dm-3: | 5750 | (alfa, 273 K) |
| 7310 | (beta, 273 K) | |
| 6973 | (m.p.) | |
| Volumen molar / cm3mol-1: | 20.65 | (alfa, 273 K) |
| 16.24 | (beta, 273 K) | |
| 17.02 | (m.p.) | |
| Resistencia eléctrica / µΩcm: | 11 | (20 °C) |
| Conductividad térmica / W m-1K-1: | 66.6 |
| Punto de fusión / °C: | 231.928 |
| Punto de ebullición / °C: | 2602 |
| Calor de fusión / kJ mol-1: | 7.2 |
| Calor de vaporización / kJ mol-1: | 296.2 |
| Calor de atomización / kJ mol-1: | 302 |
| Primera energía de ionización / kJ mol-1: | 708.58 |
| Segunda energía de ionización / kJ mol-1: | 1411.81 |
| Tercera energía de ionización / kJ mol-1: | 2943.07 |
| en la atmósfera / ppm: | - |
| en la corteza terrestre / ppm: | 2.5 |
| en los océanos / ppm: | 0.003 |
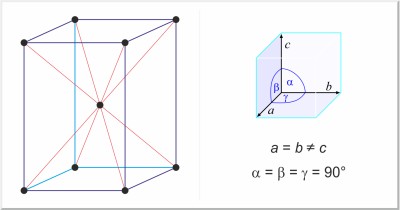
| Estructura cristalina: | tetragonal centrada en el cuerpo |
| Dimensiones de la celda unidad / pm: | a=583.16, c=318.13 |
| Grupo espacial: | I42/amd |
| Isótopo | Masa atómica relativa | Porcentaje por masa (%) |
|---|---|---|
| 112Sn | 111.904821(5) | 0.97(1) |
| 114Sn | 113.902782(3) | 0.65(1) |
| 115Sn | 114.903346(3) | 0.34(1) |
| 116Sn | 115.901744(3) | 14.53(1) |
| 117Sn | 116.902954(3) | 7.68(7) |
| 118Sn | 117.901606(3) | 24.23(11) |
| 119Sn | 118.903309(3) | 8.59(4) |
| 120Sn | 119.902197(3) | 32.59(10) |
| 122Sn | 121.903440(3) | 4.63(3) |
| 124Sn | 123.905275(1) | 5.79(5) |
| Semirreacción | Eo / V | |
|---|---|---|
| Sn4+ + 2e- → Sn2+ | +0.154 | |
| Sn4+ + 2e- → Sn2+ | +0.14 | (1 mol dm-3 HCl) |
| Sn4+ + 4e- → Sn(s) | +0.01 | |
| Sn2+ + 2e- → Sn(s) | - 0.136 | |
| Sn2+ + 2e- → Sn(s) | - 0.16 | (1 mol dm-3 HClO4) |
| SnO32- + 3H+ + 2e- → HSnO2- + H2O | +0.374 | |
| SnO32- + 6H+ + 2e- → Sn2+ + 3H2O | +0.844 | |
| HSnO2- + 3H+ + 2e- → Sn(s) + 2H2O | +0.333 | |
| Sn(s) + 4H+ + 4e- → SnH4(g) | - 1.074 |
| 49 Indio | ← | 50 Estaño | → | 51 Antimonio |
Citación de esta página:
Generalic, Eni. "Estaño." EniG. Tabla periódica de los elementos. KTF-Split, 13 Feb. 2025. Web. {Fecha de acceso}. <https://www.periodni.com/es/sn.html>.
Tablas y artículos
- Tabla periódica
- Calculadoras online
- Calculadora científica para química
- Calculadora con leyes de los gases
- Calculadora de masa molar
- Convertir ángulo
- Convertidor números romanos
- Sistema de numeración convertidor
- Preparación de las soluciones
- Etiquetado de envases químicos
- Calculadora de números de oxidacion
- ARS metodo
- Método del número de oxidación
- Método del ion-electrón
- Método de eliminación de Gauss
- Juego de memoria
- Encuentre los pares
- Tablas y artículos
- Química
- Lista de acrónimos y abreviaturas
- Sistemas cristalinos y redes de Bravais
- SGA - Pictogramas de peligro
- Diamante de peligro de NFPA 704
- Constantes físicas fundamentales
- Constantes del producto de solubilidad
- SI - Sistema Internacional de Unidades
- Composición de mezclas y soluciones
- Cálculo estequiométrico
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Ecología
- Diseño web
- Diccionario de química (inglés-croata)
- Química
- Descargas
- ≡ Menú
Copyright © 1998-2025 by Eni Generalic. Todos los derechos reservados. | Bibliografía | Disclaimer
