Ge
Germanium
GERMANIO
GRUPO DEL CARBONO
| Número atómico: | 32 |
| Grupo: | 14 |
| Periodo: | 4 |
| Configuración electrónica: | [Ar] 3d10 4s2 4p2 |
| Estados de oxidación: | +2 +4 |
| Electronegatividad: | 2.01 |
| Radio atómico / pm: | 122.5 |
| Masa atómica relativa: | 72.630(8) |
El germanio se descubrió por el químico alemán Clemens Alexander Winkler en 1866. Uno de los elementos, cuyas propiedades predijo Mendeléev (eka-silicio). Su nombre proviene de la Germania, nombre latino de Alemania. Es un semimetal gris plateado, duro y muy quebradizo con una estructura parecida a la del diamante. Se utiliza ampliamente en semiconductores. Debido a su transparencia frente a la radiación infrarroja es de gran importancia para la espectroscopia. Se obtiene de la refinación del cobre, el zinc y el plomo.
| Densidad / g dm-3: | 5323 | (293 K) |
| 5490 | (m.p.) | |
| Volumen molar / cm3mol-1: | 13.65 | (293 K) |
| 13.23 | (m.p.) | |
| Resistencia eléctrica / µΩcm: | 46000000 | (20 °C) |
| Conductividad térmica / W m-1K-1: | 59.9 |
| Punto de fusión / °C: | 938.25 |
| Punto de ebullición / °C: | 2833 |
| Calor de fusión / kJ mol-1: | 34.7 |
| Calor de vaporización / kJ mol-1: | 327.6 |
| Calor de atomización / kJ mol-1: | 373.8 |
| Primera energía de ionización / kJ mol-1: | 762.18 |
| Segunda energía de ionización / kJ mol-1: | 1537.47 |
| Tercera energía de ionización / kJ mol-1: | 3302.15 |
| en la atmósfera / ppm: | - |
| en la corteza terrestre / ppm: | 1.6 |
| en los océanos / ppm: | 0.0001 |
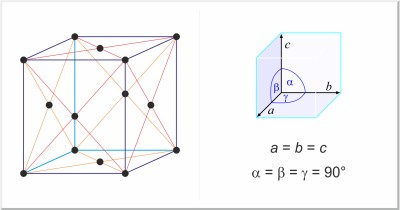
| Estructura cristalina: | cúbica centrada en las caras |
| Dimensiones de la celda unidad / pm: | a=565.754 |
| Grupo espacial: | Fd3m |
| Isótopo | Masa atómica relativa | Porcentaje por masa (%) |
|---|---|---|
| 70Ge | 69.924250(2) | 21.23(4) |
| 72Ge | 71.922076(2) | 27.66(3) |
| 73Ge | 72.923459(2) | 7.73(1) |
| 74Ge | 73.921178(2) | 35.94(2) |
| 76Ge | 75.921403(2) | 7.44(2) |
| Semirreacción | Eo / V | |
|---|---|---|
| Ge2+ + 2e- → Ge(s) | +0.00 | |
| GeO2(s) + 4H+ + 2e- → Ge2+ + 2H2O | - 0.25 | |
| GeO2(s) + 4H+ + 4e- → Ge + 2H2O | - 0.01 | |
| H2GeO3 + 4H+ + 4e- → Ge(s) + 3H2O | - 0.13 | |
| GeO(s) + 2H+ + 2e- → Ge(s) + H2O | - 0.29 |
| 31 Galio | ← | 32 Germanio | → | 33 Arsénico |
Citación de esta página:
Generalic, Eni. "Germanio." EniG. Tabla periódica de los elementos. KTF-Split, 8 Feb. 2026. Web. {Fecha de acceso}. <https://www.periodni.com/es/ge.html>.
Tablas y artículos
- Tabla periódica
- Calculadoras online
- Calculadora científica para química
- Calculadora con leyes de los gases
- Calculadora de masa molar
- Convertir ángulo
- Convertidor números romanos
- Sistema de numeración convertidor
- Preparación de las soluciones
- Etiquetado de envases químicos
- Calculadora de números de oxidacion
- ARS metodo
- Método del número de oxidación
- Método del ion-electrón
- Método de eliminación de Gauss
- Juego de memoria
- Encuentre los pares
- Tablas y artículos
- Química
- Lista de acrónimos y abreviaturas
- Sistemas cristalinos y redes de Bravais
- SGA - Pictogramas de peligro
- Diamante de peligro de NFPA 704
- Constantes físicas fundamentales
- Constantes del producto de solubilidad
- SI - Sistema Internacional de Unidades
- Composición de mezclas y soluciones
- Cálculo estequiométrico
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Ecología
- Diseño web
- Diccionario de química (inglés-croata)
- Química
- Descargas
- ≡ Menú
Copyright © 1998-2026 by Eni Generalic. Todos los derechos reservados. | Bibliografía | Disclaimer
