IDROGENO
| Numero atomico: | 1 |
| Gruppo: | 1 |
| Periodo: | 1 |
| Configurazione elettronica: | 1s1 |
| Numeri di ossidazione: | -1 +1 |
| Elettronegatività: | 2.2 |
| Raggio atomico / pm: | 37.3 |
| Massa atomica relativa: | [1.007 84, 1.008 11] |
Scopritore:1766 Sir Henry Cavendish (GB)
L'idrogeno deriva dal nome greco hydro (acqua) e gennan (generare). Esso è un gas incolore, insapore ed inodore. È l'elemento più abbondante dell'universo ed uno dei dieci più abbondanti della crosta terrestre. Lo si può trovare nelle miniere, nei pozzi di gas e di petrolio. Viene prodotto dall'industria petrolchimica. Si può anche ottenere per elettrolisi dell'acqua. E' usato come riducente nella raffinazione dei metalli e anche come propellente nei razzi. I suoi isotopi pesanti (deuterio e trizio) sono usati, rispettivamente, nella fissione e nella fusione nucleare.
| Densità / g dm-3: | 76.0 | (solido, 11 K) |
| 70.8 | (liquido, b.p.) | |
| 0.08988 | (gas, 273 K) | |
| Volume atomico / cm3mol-1: | 13.26 | (solido, 11 K) |
| 14.24 | (liquido, b.p.) | |
| 22423.54 | (gas, 273 K) | |
| Resistività Elettrica / µΩcm: | - | (20 °C) |
| Conducibilità termica / W m-1K-1: | 0.183 |
| Temperatura di fusione / °C: | -259.34 |
| Temperatura di ebollizione / °C: | 252.87 |
| Calore di fusione / kJ mol-1: | 0.12 |
| Calore di vaporizzazione / kJ mol-1: | 0.46 |
| Calore di atomizzazione / kJ mol-1: | 216.003 |
| Energia di prima ionizzazione / kJ mol-1: | 1312.06 |
| Energia di seconda ionizzazione / kJ mol-1: | - |
| Energia di terza ionizzazione / kJ mol-1: | - |
| nell'atmosfera / ppm: | 0.53 |
| nella crosta terrestre / ppm: | 1400 |
| negli oceani / ppm: | (H2O) |
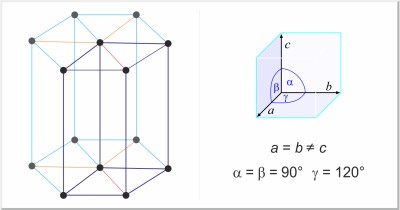
| Struttura cristallina: | esagonale |
| Dimensioni della cella unitaria / pm: | a=377.6, c=616.2 |
| Gruppo spaziale: | P63/mmc |
| Isotopo | Massa atomica relativa | Percentuale in peso (%) |
|---|---|---|
| 1H | 1.007825032(1) | 99.985(1) |
| 2H | 2.014101778(1) | 0.015(1) |
| 3H | 3.016049268(1) | * |
| Bilanciamento della semireazione | Eo / V | |
|---|---|---|
| 2H+ + 2e- → H2(g) | 0.000 | |
| 2H+ + 2e- → H2(g) | - 0.41 | ([H+] = 10-7 mol dm-3) |
| 2H+ + 2e- → H2(g) | - 0.005 | (1 mol dm-3 HCl) |
| 2H+ + 2e- → H2(g) | - 0.005 | (1 mol dm-3 HClO4) |
| 2H2O + 2e- → H2(g) + 2OH- | - 0.83 | |
| H2O2 + 2H+ + 2e- → 2H2O | +1.77 | |
| HO2- + H2O + 2e- → 3OH- | +0.88 | |
| H2(g) + 2e- → 2H- | - 2.25 |
Citazione della questa pagina:
Generalic, Eni. "Idrogeno." EniG. Tavola periodica degli elementi. KTF-Split, 8 Feb. 2026. Web. {Data di accesso}. <https://www.periodni.com/it/h.html>.
Tavoli e articoli
- Tavola periodica
- Home
- Forma breve della tavola periodica
- Forma lunga della tavola periodica
- History of the Periodic table of elements
- Tavola periodica stampabile
- Configurazione elettronica degli elementi
- Elenco alfabetico degli elementi chimici
- Naming of elements of atomic numbers greater than 100
- ASCII Tavola periodica
- Calcolatrici online
- Calcolatrice scientifica per i chimici
- Calcolatrice di leggi dei gas
- Calcolatore della massa molare
- Convertitore angolo
- Convertitore di numeri romani
- Convertitore sistemi numerazione
- Preparazione delle soluzioni
- Etichettatura dei contenitori chimici
- Calcolatrice numeri di ossidazione
- ARS metodo
- Metodo della variazione del numero di ossidazione
- Metodo ione-elettrone
- Metodo di eliminazione di Gauss
- Gioco di memoria
- Trova le coppie
- Tabelle e articoli
- Chimica
- Lista di abbreviazioni e acronimi
- Sistemi cristallini e reticoli di Bravais
- GHS - Pittogrammi di pericolo
- Diamante di fuoco di NFPA 704
- Costanti fisiche fondamentali
- Costanti del prodotto di solubilità
- SI - Unità del Sistema Internazionale
- Composizione delle miscele e soluzioni
- Calcolo stechiometrico
- Chlorinity and salinity of seawater
- Elementi di terre rare (REE)
- Ecologia
- Web design
- Dizionario di chimica (inglese-croato)
- Chimica
- Scaricare
- ≡ Menu
