Te
Tellurium
TELURIO
ANFÍGENOS
| Número atómico: | 52 |
| Grupo: | 16 |
| Periodo: | 5 |
| Configuración electrónica: | [Kr] 4d10 5s2 5p4 |
| Estados de oxidación: | -2 +4 +6 |
| Electronegatividad: | 2.1 |
| Radio atómico / pm: | 143.2 |
| Masa atómica relativa: | 127.60(3) |
El telurio fue descubierto en 1782 por el científico alemán Franz Joseph Müller von Reichenstein. Klaproth confirmó en 1798 este descubrimiento y dio al nuevo elemento su denominación que proviene de la palabra latina 'telluris', tierra. Es un sólido gris plateado, quebradizo y de carácter semimetálico. El telurio confiere dureza y resistencia a la corrosión a los aceros y aleaciones de cobre. Se usa también para dar color azul al vidrio.
| Densidad / g dm-3: | 6240 | (293 K) |
| 5797 | (m.p.) | |
| Volumen molar / cm3mol-1: | 20.45 | (293 K) |
| 22.01 | (m.p.) | |
| Resistencia eléctrica / µΩcm: | 436000 | (20 °C) |
| Conductividad térmica / W m-1K-1: | 2.35 |
| Punto de fusión / °C: | 449.51 |
| Punto de ebullición / °C: | 988 |
| Calor de fusión / kJ mol-1: | 13.5 |
| Calor de vaporización / kJ mol-1: | 104.6 |
| Calor de atomización / kJ mol-1: | - |
| Primera energía de ionización / kJ mol-1: | 869.30 |
| Segunda energía de ionización / kJ mol-1: | 1794.64 |
| Tercera energía de ionización / kJ mol-1: | 2697.75 |
| en la atmósfera / ppm: | - |
| en la corteza terrestre / ppm: | 0.01 |
| en los océanos / ppm: | - |
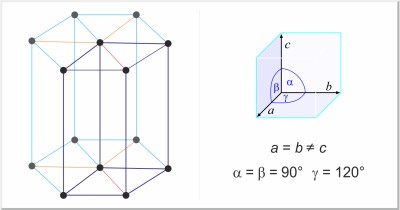
| Estructura cristalina: | hexagonal |
| Dimensiones de la celda unidad / pm: | a=445.65, c=592.68 |
| Grupo espacial: | P3121 |
| Isótopo | Masa atómica relativa | Porcentaje por masa (%) |
|---|---|---|
| 120Te | 119.90402(1) | 0.096(2) |
| 122Te | 121.903047(2) | 2.603(4) |
| 123Te | 122.904273(2) | 0.908(2) |
| 124Te | 123.902819(2) | 4.816(6) |
| 125Te | 124.904425(2) | 7.139(6) |
| 126Te | 125.903306(2) | 18.95(1) |
| 128Te | 127.904461(2) | 31.69(1) |
| 130Te | 129.906223(2) | 33.80(1) |
| Semirreacción | Eo / V | |
|---|---|---|
| Te4+ + 4e- → Te(s) | +0.568 | |
| Te4+ + 2H+ + 6e- → H2Te(g) | +0.132 | |
| TeO42- + 4H+ + 2e- → TeO2(s) + 2H2O | +1.509 | |
| HTeO4- + 3H+ + 2e- → TeO2(s) + 2H2O | +1.202 | |
| H2TeO4 + 2H+ + 2e- → TeO2(s) + 2H2O | +1.020 | |
| TeO42- + 2H+ + 2e- → TeO32- + H2O | +0.892 | |
| HTeO4- + H+ + 2e- → TeO32- + H2O | +0.584 | |
| HTeO4- + 2H+ + 2e- → HTeO3- + H2O | +0.813 | |
| H2TeO4 + H+ + 2e- → HTeO3- + H2O | +0.631 | |
| H2TeO4 + 3H+ + 2e- → HTeO2+ + 2H2O | +0.953 | |
| H2TeO4 + 6H+ + 2e- → Te4+ + 4H2O | +0.920 | |
| Te(OH)6(s) + 2H+ + 2e- → TeO2(s) + 4H2O | +1.02 | |
| TeO32- + 6H+ + 4e- → Te(s) + 3H2O | +0.827 | |
| HTeO3- + 5H+ + 4e- → Te(s) + 3H2O | +0.713 | |
| HTeO2+ + 3H+ + 4e- → Te(s) + 2H2O | +0.551 | |
| TeO2+ + 5H+ + 6e- → H2Te(g) + 2H2O | +0.121 | |
| Te(s) + 2H+ + 2e- → H2Te(g) | - 0.739 | |
| Te(s) + 2e- → Te2- | - 1.14 |
| 51 Antimonio | ← | 52 telurio | → | 53 Yodo |
Citación de esta página:
Generalic, Eni. "Telurio." EniG. Tabla periódica de los elementos. KTF-Split, 8 Feb. 2026. Web. {Fecha de acceso}. <https://www.periodni.com/es/te.html>.
Tablas y artículos
- Tabla periódica
- Calculadoras online
- Calculadora científica para química
- Calculadora con leyes de los gases
- Calculadora de masa molar
- Convertir ángulo
- Convertidor números romanos
- Sistema de numeración convertidor
- Preparación de las soluciones
- Etiquetado de envases químicos
- Calculadora de números de oxidacion
- ARS metodo
- Método del número de oxidación
- Método del ion-electrón
- Método de eliminación de Gauss
- Juego de memoria
- Encuentre los pares
- Tablas y artículos
- Química
- Lista de acrónimos y abreviaturas
- Sistemas cristalinos y redes de Bravais
- SGA - Pictogramas de peligro
- Diamante de peligro de NFPA 704
- Constantes físicas fundamentales
- Constantes del producto de solubilidad
- SI - Sistema Internacional de Unidades
- Composición de mezclas y soluciones
- Cálculo estequiométrico
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Ecología
- Diseño web
- Diccionario de química (inglés-croata)
- Química
- Descargas
- ≡ Menú
Copyright © 1998-2026 by Eni Generalic. Todos los derechos reservados. | Bibliografía | Disclaimer
