ZINC
ELEMENTOS DE TRANSICIÓN: GRUPO DEL ZINC
| Número atómico: | 30 |
| Grupo: | 12 |
| Periodo: | 4 |
| Configuración electrónica: | [Ar] 3d10 4s2 |
| Estados de oxidación: | +2 |
| Electronegatividad: | 1.65 |
| Radio atómico / pm: | 133.5 |
| Masa atómica relativa: | 65.38(2) |
Los minerales de zinc se conocian en la antigüedad, pero el zinc no fue reconocido como elemento hasta 1746, cuando el químico alemán Andreas Sigismund Marggraf aisló el metal puro calentando calamina y carbón de leña. Su nombre proviene del alto alemán zink, de zinke, punta aguda, por la forma que adoptaba al depositarse en los altos hornos. Es un metal de color blanco grisáceo, resistente a la acción del agua y el aire. En la naturaleza se encuentra, principalmente, constituyendo el mineral esfalerita (ZnS). Se emplea para recubrir el hierro (hierro galvanizado), así como en las aleaciones con el cobre (latón). El óxido de zinc, conocido como zinc blanco, se usa como pigmento en pintura.
| Densidad / g dm-3: | 7133 | (293 K) |
| 6577 | (m.p.) | |
| Volumen molar / cm3mol-1: | 9.17 | (293 K) |
| 9.94 | (m.p.) | |
| Resistencia eléctrica / µΩcm: | 5.964 | (20 °C) |
| Conductividad térmica / W m-1K-1: | 116 |
| Punto de fusión / °C: | 419.53 |
| Punto de ebullición / °C: | 907 |
| Calor de fusión / kJ mol-1: | 6.67 |
| Calor de vaporización / kJ mol-1: | 114.2 |
| Calor de atomización / kJ mol-1: | 130.181 |
| Primera energía de ionización / kJ mol-1: | 906.41 |
| Segunda energía de ionización / kJ mol-1: | 1733.31 |
| Tercera energía de ionización / kJ mol-1: | 3832.71 |
| en la atmósfera / ppm: | - |
| en la corteza terrestre / ppm: | 80 |
| en los océanos / ppm: | 0.01 |
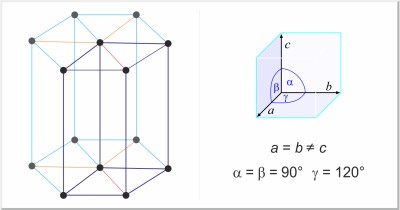
| Estructura cristalina: | hexagonal |
| Dimensiones de la celda unidad / pm: | a=266.47, c=494.69 |
| Grupo espacial: | P63/mmc |
| Isótopo | Masa atómica relativa | Porcentaje por masa (%) |
|---|---|---|
| 64Zn | 63.929147(2) | 48.6(3) |
| 66Zn | 65.926037(2) | 27.9(2) |
| 67Zn | 66.927131(2) | 4.1(1) |
| 68Zn | 67.924848(2) | 18.8(4) |
| 70Zn | 69.925325(4) | 0.6(1) |
| Semirreacción | Eo / V | |
|---|---|---|
| Zn2+ + 2e- → Zn(s) | - 0.763 | |
| ZnO22- + 4H+ + 2e- → Zn(s) + 2H2O | +0.441 | |
| HZnO2- + 3H+ + 2e- → Zn(s) + 2H2O | - 0.054 | |
| ZnO22- + 2H2O + 2e- → Zn(s) + 4OH- | - 1.216 | |
| Zn(OH)2(s) + 2e- → Zn(s) + 2OH- | - 1.245 | |
| ZnS(s) + 2e- → Zn(s) + S2- | - 1.40 | |
| Zn(NH3)42+ + 2e- → Zn(s) + 4NH3 | - 1.04 | |
| Zn(CN)42+ + 2e- → Zn(s) + 4CN- | - 1.26 |
Citación de esta página:
Generalic, Eni. "Zinc." EniG. Tabla periódica de los elementos. KTF-Split, 8 Feb. 2026. Web. {Fecha de acceso}. <https://www.periodni.com/es/zn.html>.
Tablas y artículos
- Tabla periódica
- Calculadoras online
- Calculadora científica para química
- Calculadora con leyes de los gases
- Calculadora de masa molar
- Convertir ángulo
- Convertidor números romanos
- Sistema de numeración convertidor
- Preparación de las soluciones
- Etiquetado de envases químicos
- Calculadora de números de oxidacion
- ARS metodo
- Método del número de oxidación
- Método del ion-electrón
- Método de eliminación de Gauss
- Juego de memoria
- Encuentre los pares
- Tablas y artículos
- Química
- Lista de acrónimos y abreviaturas
- Sistemas cristalinos y redes de Bravais
- SGA - Pictogramas de peligro
- Diamante de peligro de NFPA 704
- Constantes físicas fundamentales
- Constantes del producto de solubilidad
- SI - Sistema Internacional de Unidades
- Composición de mezclas y soluciones
- Cálculo estequiométrico
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Ecología
- Diseño web
- Diccionario de química (inglés-croata)
- Química
- Descargas
- ≡ Menú
