O
Oxygenium
OSSIGENO
CALCOGENI ELEMENTI
| Numero atomico: | 8 |
| Gruppo: | 16 |
| Periodo: | 2 |
| Configurazione elettronica: | [He] 2s2 2p4 |
| Numeri di ossidazione: | -2 |
| Elettronegatività: | 3.44 |
| Raggio atomico / pm: | 60.4 |
| Massa atomica relativa: | [15.999 03, 15.999 77] |
Scopritore:1772 Carl William Scheele (SE)
L'ossigeno deriva dal nome greco oxus (acido) e gennan (generare). Esso è un gas inodore, insapore e incolore. È il terzo elemento più abbondante nell'universo. È il più abbondante della crosta terrestre. Si prepara per lo più dalla distillazione frazionata dell'aria liquida. Usato nell'industria chimica ed in quella siderurgica (saldature). Utilizzato come gas medicinale.
| Densità / g dm-3: | 2000 | (solido, m.p.) |
| 1140 | (b.p.) | |
| 1.429 | (gas, 273 K) | |
| Volume atomico / cm3mol-1: | 8.00 | (solido, m.p.) |
| 14.03 | (b.p.) | |
| 22392.44 | (gas, 273 K) | |
| Resistività Elettrica / µΩcm: | - | (20 °C) |
| Conducibilità termica / W m-1K-1: | 0.0263 |
| Temperatura di fusione / °C: | -218.7916 |
| Temperatura di ebollizione / °C: | -182.95 |
| Calore di fusione / kJ mol-1: | 0.444 |
| Calore di vaporizzazione / kJ mol-1: | 6.82 |
| Calore di atomizzazione / kJ mol-1: | 246.785 |
| Energia di prima ionizzazione / kJ mol-1: | 1313.95 |
| Energia di seconda ionizzazione / kJ mol-1: | 3388.33 |
| Energia di terza ionizzazione / kJ mol-1: | 5300.51 |
| nell'atmosfera / ppm: | 209500 |
| nella crosta terrestre / ppm: | 466000 |
| negli oceani / ppm: | (H2O) |
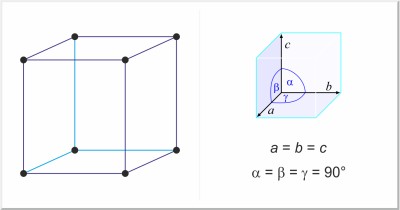
| Struttura cristallina: | cubico semplice |
| Dimensioni della cella unitaria / pm: | a=683 |
| Gruppo spaziale: | Pm3n |
| Isotopo | Massa atomica relativa | Percentuale in peso (%) |
|---|---|---|
| 16O | 15.994914622(2) | 99.762(15) |
| 17O | 16.9991315(2) | 0.038(3) |
| 18O | 17.9991604(9) | 0.200(12) |
| Bilanciamento della semireazione | Eo / V | |
|---|---|---|
| O2(g) + 4H+ + 4e- → 2H2O | +1.229 | |
| O2(g) + 4H+ + 4e- → 2H2O | +0.815 | ([H+] = 10-7 mol dm-3) |
| O2(g) + 2H2O + 4e- → 4OH- | +0.401 | |
| O2(g) + H2O + 2e- → HO2- + OH- | +0.076 | |
| O2(g) + 2H+ + 2e- → H2O2 | +0.682 | |
| O3(g) + 2H+ + 2e- → O2(g) + H2O | +2.07 | |
| O3(g) + 6H+ + 6e- → 3H2O | +1.501 | |
| O3(g) + H2O + 2e- → O2(g) + 2OH- | +1.24 | |
| HO2- + H2O + 2e- → 3OH- | +0.88 | |
| H2O2 + 2H+ + 2e- → 2H2O | +1.776 |
Citazione della questa pagina:
Generalic, Eni. "Ossigeno." EniG. Tavola periodica degli elementi. KTF-Split, 8 Feb. 2026. Web. {Data di accesso}. <https://www.periodni.com/it/o.html>.
Tavoli e articoli
- Tavola periodica
- Home
- Forma breve della tavola periodica
- Forma lunga della tavola periodica
- History of the Periodic table of elements
- Tavola periodica stampabile
- Configurazione elettronica degli elementi
- Elenco alfabetico degli elementi chimici
- Naming of elements of atomic numbers greater than 100
- ASCII Tavola periodica
- Calcolatrici online
- Calcolatrice scientifica per i chimici
- Calcolatrice di leggi dei gas
- Calcolatore della massa molare
- Convertitore angolo
- Convertitore di numeri romani
- Convertitore sistemi numerazione
- Preparazione delle soluzioni
- Etichettatura dei contenitori chimici
- Calcolatrice numeri di ossidazione
- ARS metodo
- Metodo della variazione del numero di ossidazione
- Metodo ione-elettrone
- Metodo di eliminazione di Gauss
- Gioco di memoria
- Trova le coppie
- Tabelle e articoli
- Chimica
- Lista di abbreviazioni e acronimi
- Sistemi cristallini e reticoli di Bravais
- GHS - Pittogrammi di pericolo
- Diamante di fuoco di NFPA 704
- Costanti fisiche fondamentali
- Costanti del prodotto di solubilità
- SI - Unità del Sistema Internazionale
- Composizione delle miscele e soluzioni
- Calcolo stechiometrico
- Chlorinity and salinity of seawater
- Elementi di terre rare (REE)
- Ecologia
- Web design
- Dizionario di chimica (inglese-croato)
- Chimica
- Scaricare
- ≡ Menu
Copyright © 1998-2026 by Eni Generalic. Tutti i diritti sono riservati. | Bibliografia | Disclaimer
