SÉLÉNIUM
CHALCOGÈNE
| Nombre atomique: | 34 |
| Groupe: | 16 |
| Période: | 4 |
| Configuration électronique: | [Ar] 3d10 4s2 4p4 |
| Nombre d'oxydation: | -2 +4 +6 |
| Électronégativité: | 2.55 |
| Rayon atomique / pm: | 116 |
| Masse atomique relatives: | 78.971(8) |
Le sélénium a été découvert par Jöns Jacob Berzelius (SE) en 1817. Étymologie du nom: vient du grec selene signifiant lune. Le sélénium est un métalloïde mou, analogue au soufre. Son aspect est variable: entre celui d'un métal gris et celui d'un verre rouge. Il ne réagit pas avec l'eau. Il brûle dans l'air. Il réagit avec les bases et l'acide nitrique. Il est toxique par inhalation et ingestion. Le sélénium est obtenu à partir du raffinage du plomb, du cuivre et du nickel. Grâce à la lumière le sélénium devient conducteur de l'électricité. Il est utilisé dans piles photoélectriques, les cameras de TV, la xérographie et comme semi-conducteur dans les batteries solaires et les redresseurs. Il colore le verre en rouge.
| Densité / g dm-3: | 4790 | (gris, 293 K) |
| 3987 | (m.p.) | |
| Volume molaire / cm3mol-1: | 16.48 | (gris, 293 K) |
| 19.80 | (m.p.) | |
| Résistivité électrique / µΩcm: | 12 | (20 °C) |
| Conductibilité thermique / W m-1K-1: | 2.04 |
| Point de fusion / °C: | 221 |
| Point d'ébullition / °C: | 685 |
| Enthalpie de fusion / kJ mol-1: | 5.1 |
| Enthalpie d'évaporation / kJ mol-1: | 90 |
| Chaleur d'atomisation / kJ mol-1: | 226.4 |
| Energie de première ionisation / kJ mol-1: | 940.97 |
| Energie de deuxième ionisation / kJ mol-1: | 2044.54 |
| Energie de troisième ionisation / kJ mol-1: | 2973.74 |
| dans l'atmosphère / ppm: | - |
| dans la croute terrestre / ppm: | 0.05 |
| dans les océans / ppm: | - |
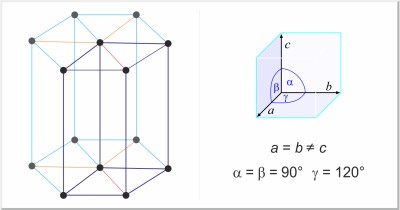
| Structure cristalline: | hexagonal |
| Dimension de la cellule unitaire / pm: | a=436.56, c=495.90 |
| Groupe d'espace: | P3121 |
| Isotope | Masse atomique relatives | Pourcentage massique (%) |
|---|---|---|
| 74Se | 73.922477(2) | 0.89(2) |
| 76Se | 75.919214(2) | 9.36(11) |
| 77Se | 76.919915(2) | 7.63(6) |
| 78Se | 77.917310(2) | 23.78(9) |
| 80Se | 79.916522(2) | 49.61(10) |
| 82Se | 81.916700(2) | 8.73(6) |
| Demi-réaction | Eo / V | |
|---|---|---|
| SeO42- + 2H+ + 2e- → SeO32- + H2O | +0.880 | |
| SeO42- + H2O + 2e- → SeO32- + 2OH- | +0.05 | |
| SeO42- + 3H+ + 2e- → HSeO3- + H2O | +1.075 | |
| SeO42- + 4H+ + 2e- → H2SeO3 + H2O | +1.15 | |
| HSeO4- + 3H+ + 2e- → H2SeO3 + H2O | +1.090 | |
| SeO32- + 6H+ + 4e- → Se(s) + 3H2O | +0.875 | |
| HSeO3- + 5H+ + 4e- → Se(s) + 3H2O | +0.778 | |
| H2SeO3 + 4H+ + 4e- → Se(s) + 3H2O | +0.740 | |
| SeO32- + 6H+ + 6e- → Se2- + 3H2O | +0.276 | |
| SeO32- + 7H+ + 6e- → HSe- + 3H2O | +0.414 | |
| HSeO3- + 6H+ + 6e- → HSe- + 3H2O | +0.349 | |
| HSeO3- + 7H+ + 6e- → H2Se(g) + 3H2O | +0.386 | |
| H2SeO3 + 6H+ + 6e- → H2Se(g) + 3H2O | +0.360 | |
| Se(s) + 2H+ + 2e- → H2Se(g) | - 0.369 | |
| Se(s) + 2e- → Se2- | - 0.924 | |
| Se(s) + H+ + 2e- → HSe- | - 0.510 | |
| Se(s) + 2H+ + 2e- → H2Se(g) | - 0.399 |
| 33 Arsenic | ← | 34 Sélénium | → | 35 Brome |
Citation de cette page:
Generalic, Eni. "Sélénium." EniG. Tableau périodique des éléments. KTF-Split, 13 Feb. 2025. Web. {Date de l'accès}. <https://www.periodni.com/fr/se.html>.
Tableaux et articles
- Tableau périodique
- Home
- Forme courte du tableau périodique
- Forme longue du tableau périodique
- History of the Periodic table of elements
- Impression du tableau périodique
- Configuration électronique des éléments
- Liste alphabétique des éléments chimiques
- Naming of elements of atomic numbers greater than 100
- ASCII Tableau périodique
- Calculatrices online
- Calculatrice scientifique pour chimiste
- Calculatrice lois de gaz
- Calculateur de masse molaire
- Convertir angle
- Convertisseur chiffres romains
- Convertisseur systèmes numériques
- Préparation des solutions
- Étiquetage des conteneurs chimiques
- Calculateur de nombres d'oxydation
- ARS methode
- Méthode du changement des nombres d'oxydation
- Méthode ions-électrons
- Méthode d'élimination de Gauss
- Jeu de mémoire
- Trouvez les paires
- Tableaux et articles
- Chimie
- Liste des abréviations et acronymes
- Systèmes cristallins et réseaux de Bravais
- SGH - Pictogrammes de danger
- NFPA 704 feu diamant
- Constantes physiques fondamentales
- Constantes du produit de solubilité
- SI - Système international d'unités
- Composition des melanges et des solutions
- Calcul stœchiométrique
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Écologie
- Web design
- Dictionnaire de chimie (anglais-croate)
- Chimie
- Télécharger
- ≡ Menu
